(单选题)物质的结构决定性质,微粒间的相互作用力越强,熔点越高。一些氧化物的熔点如下表:
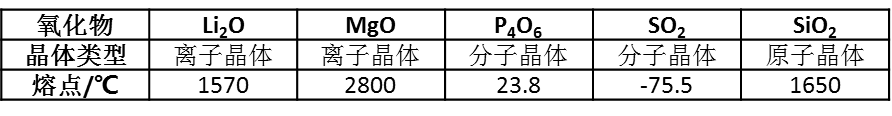
下列选项中,不能解释氧化物熔点存在差异的是:
A.分子晶体中的作用力是相对较弱的分子间作用力
B.离子晶体中的作用力是相对较强的离子键
C.原子晶体中的作用力是相对较弱的共价键
D.Li2O中的离子键弱于MgO的
解析
第一步,确定题型。
本题考查化学中的熔点。
第二步,分析原理。
![]()
A项:分子晶体是分子间通过分子间作用力(分子间作用力又名范德华力,而氢键不是化学键,是一种特殊的分子间作用力,属于分子间作用力)构成的晶体,如表中的和,作用力较弱,熔沸点较低,因此可以解释氧化物的熔点差异;
![]()
B项:离子晶体是正、负离子通过离子键结合形成的晶体,如表中的和MgO,作用力较强,熔沸点较高,因此可以解释氧化物的熔点差异;
![]()
C项:原子晶体是相邻原子之间只通过共价键结合而成的晶体,如表中的,作用力较强,熔沸点较高,C项表述错误,不能解释氧化物的熔点差异;
![]()
D项:和MgO均为离子晶体,离子间相互作用力均为离子键,MgO的熔点较高,根据“微粒间的相互作用力越强,熔点越高”,其离子键较强,因此可以解释氧化物的熔点差异。
因此,选择C选项。
在了解相关国考试题后,考生可积极备考24年国家公务员考试,成功的关键是有效的备考!










